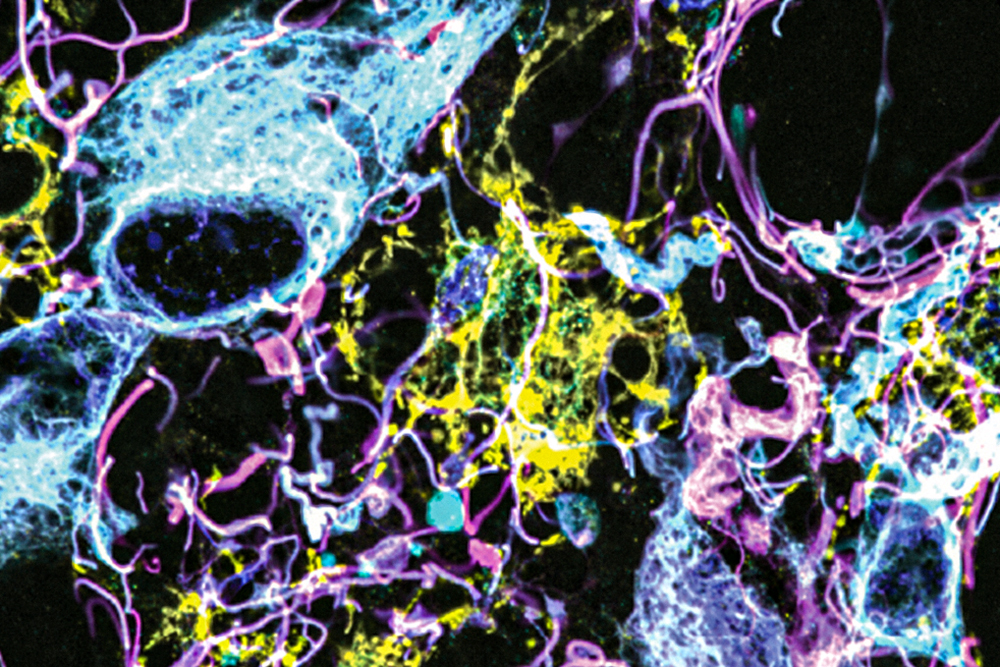
با استفاده از یک تکنیک میکروسکوپی جدید، محققان MIT و Brigham and Women’s Hospital/ دانشکده پزشکی هاروارد، بافت مغز انسان را با جزئیات بیشتری نسبت به گذشته تصویربرداری کردند و سلولها و ساختارهایی را که قبلاً قابل مشاهده نبودند، آشکار کردند.
در میان یافتههای خود، محققان دریافتند که برخی از تومورهای مغزی “درجه پایین” حاوی سلولهای تومور تهاجمی مشکوکتر از حد انتظار هستند، که نشان میدهد برخی از این تومورها ممکن است تهاجمیتر از آنچه قبلا تصور میشد باشند.
محققان امیدوارند که این روش در نهایت بتواند برای تشخیص تومورها، ایجاد پیشبینیهای دقیقتر و کمک به پزشکان در انتخاب روشهای درمانی استفاده شود.
ما شروع به دیدن این موضوع کردهایم که تعاملات نورونها و سیناپسها با مغز اطراف چقدر برای رشد و پیشرفت تومورها مهم است. پابلو والدز، فوق دکترای سابق MIT که اکنون دستیار است، میگوید بسیاری از این چیزها را واقعاً نمیتوانستیم با ابزارهای معمولی ببینیم، اما اکنون ابزاری برای بررسی این بافتها در مقیاس نانو و تلاش برای درک این تعاملات داریم. استاد عصب شناسی در واحد پزشکی دانشگاه تگزاس و نویسنده اصلی این مطالعه.
ادوارد بویدن، پروفسور ایوا تان، استاد نوروتکنولوژی در MIT. استاد مهندسی زیست شناسی، هنر و علوم رسانه، و علوم مغز و شناختی؛ محققی در موسسه پزشکی هاوارد هیوز؛ و یکی از اعضای موسسه تحقیقات مغز MIT McGovern و موسسه تحقیقات سرطان یکپارچه Koch. و E. Antonio Ciocca، استاد جراحی مغز و اعصاب در دانشکده پزشکی هاروارد و رئیس جراحی مغز و اعصاب در Brigham and Women’s Hospital، نویسندگان اصلی این مطالعه هستند. امروز ظاهر می شود که در پزشکی ترجمه علمی.
قابل مشاهده کردن مولکول ها
روش تصویربرداری جدید بر اساس میکروسکوپ انبساطروشی که در سال 2015 در آزمایشگاه Boyden بر اساس یک فرض ساده توسعه یافت: به جای استفاده از میکروسکوپ های قدرتمند و گران قیمت برای به دست آوردن تصاویر با وضوح بالا، محققان راهی برای گسترش خود بافت ابداع کردند که به آن اجازه می دهد با وضوح بسیار بالا تصویربرداری شود. میکروسکوپ نوری معمولی
این تکنیک با قرار دادن بافت در پلیمری کار میکند که با افزودن آب متورم میشود و سپس پروتئینهایی را که معمولاً بافت را کنار هم نگه میدارند، نرم میکند و تجزیه میکند. سپس افزودن آب، پلیمر را متورم می کند و تمام پروتئین ها را از هم جدا می کند. این بزرگنمایی بافت به محققان امکان می دهد تصاویری با وضوح حدود 70 نانومتر به دست آورند که قبلا فقط با میکروسکوپ های بسیار تخصصی و گران قیمت مانند میکروسکوپ های الکترونی روبشی امکان پذیر بود.
سال 2017 شاهد توسعه آزمایشگاه بویدن بودیم راه گسترش نمونههای بافت انسانی را حفظ کردند، اما معرفهای شیمیایی که آنها استفاده میکردند، پروتئینهایی را که محققان علاقهمند به برچسبگذاری آنها بودند نیز از بین بردند. با برچسب گذاری پروتئین ها با آنتی بادی های فلورسنت قبل از انبساط، می توان مکان و هویت پروتئین ها را پس از تکمیل فرآیند انبساط مشاهده کرد. با این حال، آنتیبادیهایی که معمولاً برای این نوع برچسبگذاری مورد استفاده قرار میگیرند، نمیتوانند به راحتی از بافت بستهبندی شده قبل از منبسط شدن عبور کنند.
بنابراین، برای این مطالعه، نویسندگان پروتکل متفاوتی برای نرم کردن بافت ایجاد کردند که بافت را تجزیه میکند اما پروتئینهای موجود در نمونه را حفظ میکند. پس از انبساط بافت، پروتئین ها را می توان با آنتی بادی های فلورسنت تجاری موجود برچسب گذاری کرد. سپس محققان می توانند چندین دور تصویربرداری را با سه یا چهار پروتئین مختلف در هر دور انجام دهند. این برچسبگذاری پروتئینها، تصویربرداری از ساختارهای بیشتری را ممکن میسازد، زیرا وقتی بافت منبسط شد، آنتیبادیها میتوانند از آن عبور کنند و پروتئینهایی را که قبلاً نمیتوانستند به آنها برسند برچسبگذاری کنند.
والدز میگوید: «ما فضای بین پروتئینها را باز میکنیم تا بتوانیم آنتیبادیها را به فضاهای شلوغ وارد کنیم که در غیر این صورت نمیتوانستیم. ما دیدیم که میتوانیم بافت را گسترش دهیم، میتوانیم پروتئینها را حذف کنیم، و میتوانیم با انجام چندین دور رنگآمیزی از پروتئینهای بسیار زیادی در همان بافت تصویربرداری کنیم.»
محققان با همکاری با پروفسور دبلینا سارکار، دستیار MIT، نوعی از این «کاهش» را در سال 2022 با استفاده از بافت موش نشان دادند.
مطالعه جدید منجر به یک تکنیک تخلیه برای استفاده با نمونههای بافت مغز انسان شد که در تنظیمات بالینی برای تشخیص پاتولوژیک و هدایت تصمیمهای درمانی استفاده میشوند. کار با این نمونهها میتواند دشوارتر باشد، زیرا معمولاً در پارافین قرار میگیرند و با مواد شیمیایی دیگری که باید قبل از منبسط شدن بافت تجزیه شوند، درمان میشوند.
در این مطالعه، محققان تا 16 مولکول مختلف را در هر نمونه بافت برچسب گذاری کردند. مولکول هایی که آنها هدف قرار دادند شامل نشانگرهایی برای ساختارهای مختلف، از جمله آکسون ها و سیناپس ها، و همچنین نشانگرهایی بود که انواع سلول ها مانند آستروسیت ها و سلول هایی را که رگ های خونی را تشکیل می دهند، شناسایی می کردند. آنها همچنین مولکول های مرتبط با تهاجمی تومور و تخریب عصبی را برچسب گذاری کردند.
با استفاده از این رویکرد، محققان بافت سالم مغز را به همراه نمونههایی از بیماران مبتلا به دو نوع گلیوم – گلیوبلاستوما با درجه بالا، که تهاجمیترین تومور اولیه مغزی با پیشآگهی ضعیف است، و گلیومهای درجه پایین، که کمتر تهاجمی هستند، تجزیه و تحلیل کردند. .
ما میخواستیم تومورهای مغزی را بررسی کنیم تا بتوانیم آنها را در مقیاس نانو بهتر درک کنیم و در نتیجه بتوانیم درمانها و تشخیصهای بهتری در آینده ایجاد کنیم. والدز میگوید: در آن مرحله، بیشتر در مورد توسعه ابزاری بود تا بتوانیم آنها را بهتر درک کنیم، زیرا در حال حاضر در عصب انکولوژی، مردم از نظر تصویربرداری با وضوح فوقالعاده کار زیادی انجام ندادهاند.
ابزار تشخیصی
برای شناسایی سلول های تومور تهاجمی در گلیوماهای مورد مطالعه، محققان ویمنتین، پروتئینی را که در گلیوبلاستوم های بسیار تهاجمی یافت می شود، برچسب گذاری کردند. در کمال تعجب، آنها سلولهای تومور بیانکننده ویمنتین را در گلیوماهای با درجه پایین بسیار بیشتر از آنچه با استفاده از هر روش دیگری مشاهده شده بود، یافتند.
والدز میگوید: «این چیزی در مورد بیولوژی این تومورها به ما میگوید، به ویژه اینکه چگونه برخی از آنها احتمالاً ماهیت تهاجمیتر از آن چیزی هستند که شما با استفاده از تکنیکهای رنگآمیزی استاندارد گمان میکنید.»
هنگامی که بیماران گلیوما تحت عمل جراحی قرار میگیرند، نمونههای تومور حفظ و با استفاده از رنگآمیزی ایمونوهیستوشیمی مورد تجزیه و تحلیل قرار میگیرند، که میتواند نشانگرهای خاصی از پرخاشگری، از جمله برخی از نشانگرهای تحلیل شده در این مطالعه را نشان دهد.
اینها سرطانهای مغز غیرقابل درمان هستند و این نوع اکتشافات به ما این امکان را میدهند که بفهمیم کدام مولکولهای سرطانی را هدف قرار دهیم تا بتوانیم درمانهای بهتری طراحی کنیم.» Ciocca میگوید: این همچنین تأثیر عمیق پزشکانی مانند ما در Brigham و Women’s را در تعامل با دانشمندان پایه مانند Ed Boyden در MIT برای کشف فناوریهای جدیدی که میتواند زندگی بیماران را بهبود بخشد، نشان میدهد.
محققان امیدوارند که تکنیک میکروسکوپ بزرگنمایی آنها به پزشکان اجازه دهد تا اطلاعات بیشتری در مورد تومورهای بیماران بیاموزند و به آنها کمک کند تا میزان تهاجمی بودن تومور را تعیین کنند و انتخاب های درمانی را راهنمایی کنند. والدز اکنون قصد دارد یک مطالعه بزرگتر در مورد انواع تومور انجام دهد تا سعی کند دستورالعمل های تشخیصی را بر اساس ویژگی های تومور ایجاد کند که می توان با استفاده از این روش آشکار کرد.
او میگوید: «امیدواریم که این یک ابزار تشخیصی برای تشخیص سلولهای نشانگر، فعل و انفعالات و غیره باشد که قبلاً نمیتوانستیم. این یک ابزار کاربردی است که به دنیای بالینی نوروآنکولوژی و آسیب شناسی عصبی کمک می کند تا به بیماری های عصبی در مقیاس نانو نگاه کند، زیرا در واقع ابزاری بسیار ساده برای استفاده است.
آزمایشگاه Boyden همچنین قصد دارد از این تکنیک برای مطالعه سایر جنبه های عملکرد مغز در بافت های سالم و بیمار استفاده کند.
بویدن میگوید: «توانایی انجام تصویربرداری نانو مهم است زیرا زیستشناسی در مورد چیزهای در مقیاس نانو – ژنها، محصولات ژنی، مولکولهای زیستی- است و آنها در فواصل نانومقیاس برهم کنش دارند. ما میتوانیم انواع فعل و انفعالات در مقیاس نانو، از جمله تغییرات سیناپسی، فعل و انفعالات ایمنی، و تغییراتی را که در طول سرطان و پیری رخ میدهند، مطالعه کنیم.
این تحقیق توسط K. Lisa Yang، مؤسسه پزشکی هوارد هیوز، جان دوئر، بشردوستانه باز، بنیاد بیل و ملیندا گیتس، برنامه تحقیقات مرزی مؤسسه کخ، مؤسسه ملی بهداشت، و بنیاد تحقیقات و آموزش جراحی مغز و اعصاب تأمین شده است. .


